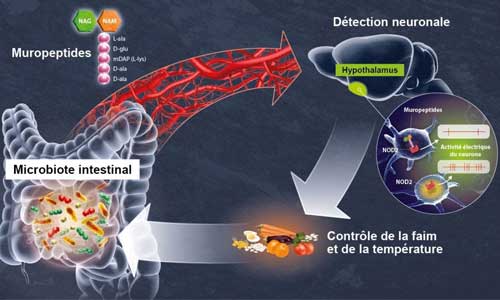
Et si notre microbiote intestinal (l'ensemble des micro-organismes qui évoluent le long de notre système digestif) communiquait avec notre cerveau ? Des scientifiques de l'Institut Pasteur, de l'Inserm et du CNRS, trois organismes français de recherche, ont découvert, dans un modèle animal, que des neurones de l'hypothalamus (centre de contrôle de fonctions telles que la faim, le stress ou l'éveil) détectent directement les variations de l'activité bactérienne de l'intestin et adaptent l'appétit et la température corporelle en conséquence. « Des produits dérivés du microbiote intestinal se retrouvent dans la circulation sanguine et modulent les processus physiologiques de l'hôte, tels que l'immunité, le métabolisme et les fonctions cérébrales », détaillent-ils. Ces résultats, prometteurs pour de nouvelles approches thérapeutiques contre les troubles métaboliques, tels que le diabète ou l'obésité, seront publiés dans la revue scientifique américaine Science le 15 avril 2022.
Importance de l'axe intestin-cerveau
Le microbiote intestinal constitue le plus grand réservoir de bactéries de l'organisme. De plus en plus de travaux mettent en évidence son lien de dépendance avec son hôte (l'Homme) et soulignent l'importance de l'axe intestin-cerveau. Pour comprendre comment ces bactéries peuvent avoir un effet direct sur l'activité de certains neurones du cerveau, le consortium de scientifiques s'est particulièrement intéressé au « récepteur » NOD2, présent à l'intérieur des cellules, en particulier immunitaires. Son rôle : détecter la présence de muropeptides, des composés des parois bactériennes, qui peuvent être considérés comme les produits dérivés du microbiote intestinal.
Risque supérieur de diabète de type 2
Présents dans l'intestin, le sang et le cerveau, les muropeptides sont libérés par les bactéries lorsqu'elles prolifèrent. « Quand le récepteur NOD2 est défaillant, les neurones ne sont plus réprimés par les muropeptides ; le cerveau perd alors le contrôle de la prise alimentaire et de la température corporelle, observent les auteurs de l'étude. En conséquence, les souris prennent du poids et sont plus susceptibles de développer un diabète de type 2, en particulier chez les femelles âgées. » Les scientifiques ont ainsi montré que ce sont ici les neurones qui perçoivent directement les muropeptides bactériens, « une tâche généralement dévolue aux cellules du système immunitaire », indiquent-ils. Une découverte « étonnante » et « stupéfiante », selon eux.
Vers de nouvelles thérapies ?
Ainsi, les neurones semblent détecter l'activité bactérienne (la prolifération et la mort) pour mesurer directement l'impact de l'alimentation sur l'écosystème intestinal. « Il est possible qu'une prise alimentaire excessive ou un aliment particulier favorise l'expansion exagérée de certaines bactéries ou de pathogènes et mette ainsi en danger l'équilibre intestinal », souligne Gérard Eberl, responsable de l'unité Microenvironnement et immunité à l'Institut Pasteur (Inserm). Etant donné l'impact des muropeptides sur les neurones de l'hypothalamus et le métabolisme, les chercheurs s'interrogent désormais sur leur rôle dans d'autres fonctions du cerveau, afin de comprendre l'association entre certaines pathologies cérébrales et les variants génétiques de NOD2. Cette découverte ouvre la voie à de nouveaux projets interdisciplinaires pour les trois équipes et, à terme, à de nouvelles approches thérapeutiques notamment pour les maladies du cerveau, telles que l'épilepsie, Alzheimer, Parkinson ou encore la sclérose en plaques.
Autisme : greffe de selles pour diminuer les symptômes
Depuis plusieurs années, des travaux s'intéressent à l'impact de la flore intestinale sur le cerveau chez les personnes avec autisme (articles complets en lien ci-dessous). En introduisant des bactéries (Lactobacillus reuteri) dans les intestins de rongeurs, des chercheurs américains ont pu inverser des déficits de comportements sociaux qui rappellent les symptômes de ce trouble neuro-développemental. En 2019, d'autres scientifiques ont mis en lumière une approche inédite, trivialement appelée « la greffe de selles », pour diminuer notamment les difficultés communicationnelles, les stéréotypies ainsi que les complications gastro-intestinales (article en lien ci-dessous).
© Institut Pasteur / Pascal Marseaud