« Aujourd'hui marque un tournant dans la recherche sur la sclérose latérale amyotrophique (SLA) ». C'est par ces mots porteurs d'espoir que Christopher A. Viehbacher, CEO de l'entreprise pharmaceutique Biogen, a annoncé le 28 avril 2023 la nouvelle : la Food and drugs administration (FDA) (l'équivalent de notre Agence nationale de sécurité du médicament) vient d'autoriser la mise en circulation d'un traitement contre la SLA, aussi appelée maladie de Charcot, chez les adultes présentant une mutation du gène SOD1 (superoxide dismutase 1), qui touche environ 330 personnes aux États-Unis et moins d'un millier en Europe.
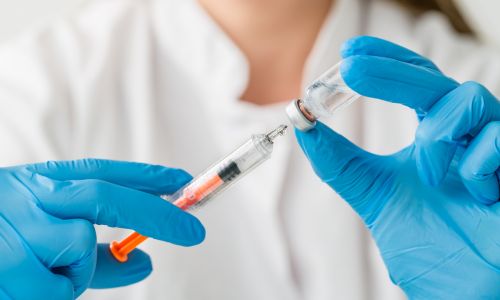
Qalsody en injection
Son nom ? Le « Qalsody » ( tofersen). Le médicament, prescrit en injection de 100 mg/15 ml, a montré de bons résultats dans le ralentissement de cette maladie neurodégénérative progressive et mortelle en agissant sur le taux plasmatique de neurofilaments à chaîne légère (NfL), un biomarqueur de la neurodégénérescence. Cette autorisation de mise sur le marché a été obtenue à la suite de plusieurs essais cliniques concluants, menés en 2022 durant 28 semaines sur des patients âgés de 23 à 78 ans présentant une faiblesse musculaire associée à la SLA et une mutation du gène SOD1 confirmée en laboratoire.
Amélioration de la fonction motrice et pulmonaire
Les chercheurs de l'Université de Sheffield, en Angleterre, ont alors constaté que ce traitement avait réduit significativement les niveaux de la protéine défectueuse (la SOD1), améliorant la fonction motrice et pulmonaire des patients. Néanmoins, quelques mises en garde et précautions d'emploi portent sur des évènements neurologiques graves, dont des cas de myélite et/ou radiculopathie, d'œdème papillaire, d'hypertension intracrânienne et de méningite aseptique et peuvent conduire à arrêter ou interrompre le traitement de manière temporaire. Certains effets indésirables sont également observés chez 10 % ou plus des patients : douleurs, fatigue intense, arthralgie, taux élevé de leucocytes dans le liquide cérébrospinal (LCS) et myalgie.
« L'autorisation du Qalsody octroyée par la FDA me donne l'espoir que les personnes atteintes par cette forme rare puissent voir le déclin de leur force, de leur fonction physique et de leur fonction respiratoire ralentir », s'est réjoui Timothy M. Miller, impliqué dans les recherches. Son étude a été publiée en septembre 2022 dans le National library of medicine.
2 % ont la mutation génétique SOD1
15 % de personnes atteintes de la maladie de Charcot présentent aujourd'hui une forme génétique de la maladie (une forme familiale) et 2 % ont la mutation génétique SOD1, précisément ciblée par le tofersen. Voilà trente ans que le SOD1 a été identifié comme cause de la SLA. Depuis, des recherches scientifiques étaient menées sans relâche pour trouver des traitements ciblant les facteurs génétiques. « La confirmation du bénéfice clinique lors d'essais confirmatoires pourrait donner lieu à une autorisation permanente », précise Biogen, qui se présente comme « pionnière » dans la recherche sur cette maladie. L'étude « de phase 3 ATLAS » actuellement en cours, qui vise à évaluer le tofersen chez les personnes présymptomatiques porteuses de la mutation SOD1 sera considérée comme « essai confirmatoire », poursuit-elle. En Europe, l'Agence européenne du médicament (EMA) a accepté d'examiner la demande d'autorisation de mise sur le marché (AMM) de tofersen, au mois de décembre 2022. La procédure est en cours.
Quid des autres formes de la maladie ?
Reste aujourd'hui à trouver des traitements pour les autres formes génétiques ou non de la maladie, qui représentent encore la majorité des cas. « Nous sommes convaincus que cette avancée scientifique importante donnera une impulsion supplémentaire au développement de médicaments innovants contre la SLA », conclut Christopher A. Viehbacher. De grands espoirs reposent à ce titre sur un autre médicament en cours de développement, lui aussi proposé par Biogen, le « BIIB105 », qui agirait sur une autre mutation génétique de la maladie, l'ataxine-2 (ATXN2).